![]()
FAQ Entsäuerung von Trinkwasser mit Calciumkarbonat, Marmorkies oder Dolomit
- 1. Wozu Entsäuerung von Trinkwasser?
- 2. Einsatzgebiete von Anlagen zur Entsäuerung
- 3. Methoden der Entsäuerung von Trinkwasser
- 4. Prinzip der Entsäuerung in geschlossenen Schnellfiltern
- 5. Woher kommt unser Calciumcarbonat
- 6. Mögliche Probleme bei der Entsäuerung von Trinkwasser
- 7. Welcher Anlagentyp soll es sein
- 8. Was ist sonst noch beim Einsatz von Entsäuerungsanlagen zu beachten?
- 9. Zu den Produktseiten der Entsäuerungsanlagen mit Schnellfiltern
1. Wozu Entsäuerung
Wasser wurde in früheren Zeiten in drucklosen Wasserführungssystemen transportiert. So gilt z.B. das Wasserleitungssystem des römischen Reiches bis heute als Spitzenleistung der Ingenieurskunst. Die sichere Wasserversorgung trug wesentlich zum Aufstieg Roms als abendländische Großmacht bei.
Das in den Aquaedukten (im Bild: Pont du Gare) geführte Wasse r
fließt in einem mehr oder weniger starkem Gefälle, zum Teil auch in offen
ausgeführten Rinnen, zu den Wasserverbrauchern. Dadurch hat das Wasser
einerseits Zeit Sauerstoff aufzunehmen, andererseits werden Gase wie
Kohlendioxid ausgetrieben. Die Wasserbeschaffenheit ähnelt daher einem
natürlichen Wasser, d.h. es herrscht weitestgehend ein Gleichgewicht zwischen im
Wasser gelösten Gasen, namentlich das Kohlendioxid und gelösten Inhaltsstoffen
wie Calcium.
r
fließt in einem mehr oder weniger starkem Gefälle, zum Teil auch in offen
ausgeführten Rinnen, zu den Wasserverbrauchern. Dadurch hat das Wasser
einerseits Zeit Sauerstoff aufzunehmen, andererseits werden Gase wie
Kohlendioxid ausgetrieben. Die Wasserbeschaffenheit ähnelt daher einem
natürlichen Wasser, d.h. es herrscht weitestgehend ein Gleichgewicht zwischen im
Wasser gelösten Gasen, namentlich das Kohlendioxid und gelösten Inhaltsstoffen
wie Calcium.
Beide genannten Stoffe binden sich in einem ganz bestimmten Verhältnis. Ist
dieses Verhältnis im Gleichgewicht, ist das Wasser weder aggressiv gegenüber
Umgebungsmaterialien noch können Kalkausfällungen das Leitungssystem
beeinträchtigen.
Probleme gibt es immer dann, wenn Wasser keine Gelegenheit bekommt, dieses Kalk-Kohlensäure-Gleichgewicht herzustellen. Dies ist regelmäßig dann der Fall, wenn Wasser in geschlossenen Rohrleitungssystemen befördert wird. Hier kann nun entweder die freie Kohlensäure Rohrwandungen angreifen oder ausfällender Kalk verblockt die Rohre. Dadurch sind in den Anfängen der zentralen Wasserversorgung beachtliche Schäden durch Korrosion oder Kalkablagerungen entstanden.
Grundsätzlich lässt sich vereinfacht sagen:
Ist Wasser kalklösend, so wirkt es korrosiv. Kalk-Rost-Schutzschichten in Stahl
und Gussrohren werden aufgelöst und führen zum Lochfraß oder Flächenkorrosion
mit der Folge von Rohrbrüchen. Insbesondere bei sauren Wässern in
Verbindung mit verzinkten Leitungen, Kupfer- oder Bleileitungen Rohrleitungen
können gesundheitliche Beeinträchtigungen durch die in das Wasser eingetragenen
Schwermetall-Ionen erwachsen. Bei Zementwerkstoffen können durch calcitlösende
Wässer die Festigkeit beeinträchtigen, da die darin enthaltenen
Calciumkarbonatanteile aufgelöst werden.
Ist Wasser dagegen kalkabscheidend, dann führt dies zu Ablagerungen in Rohrleitungen und Anlagen. Solches Wasser kann Filter verbacken, Warmwasserbereiter beschädigen und Rohrleitungen verstopfen.
Das Kalk-Kohlensäure-Gleichgewicht ist stark von der Wassertemperatur abhängig. Nahezu jeder wird beim Erwärmen von Nudelwasser oder Kaffeewasser das Ausfällen zu Kalk beobachtet beobachtet haben können
Anlagen zur Entsäuerung von Wasser dienen also dem Schutz von Rohrleitungen und Armaturen vor Korrosion.
2. Einsatzgebiete von Entsäuerungsanlagen
- Trinkwasseraufbereitung in der öffentlichen Wasserversorgung
- private Brunnenwasserversorgung
- Entsäuerung/Entgasung für technische Bereiche wie Kraftwerke, Heizungsanlagen, Dampfkessel
- Kühlwasseraufbereitung
3. Methoden der Entsäuerung
Die in dieser FAQ angesprochenen Methoden zur Entsäuerung von Wasser befassen sich mit der chemischen Neutralisation der freien überschüssigen Kohlensäure. Das Ziel dieser Aufbereitung (nur Trinkwasser!) ist das Erreichen des Kalk-Kohlensäure-Gleichgewichtes.
Dieses Gleichgewicht lässt sich in vielen Fällen entweder mittels Dosierung von Natronlauge oder aber über Filtration von kalkhaltigen Granulaten wie Calciumkarbonat, Jurakalk, Marmorkies oder Dolomit erreichen.
Die Filtration über Granulate wird oftmals in der Trinkwasseraufbereitung eingesetzt und ist insbesondere für den Privatanwender die einfachste Möglichkeit, sein Brunnenwasser in den Griff zu bekommen.
Er wird sie möglichst immer dann anwenden, wenn in der Wasseranalyse
sinngemäß steht:
- Wasser ist korrosiv
- Wasser ist calcitlösend
- Calciumkarbonat-Sättigung ist nicht gegeben
- SI (=Sättigungsindex) < 0
Weiter Themenanfang Seitenanfang
4. Prinzip der Entsäuerung in geschlossenen Schnellfiltern
Weiter Themenanfang Seitenanfang
5. Woher kommt unser Calciumcarbonat
Weiter Themenanfang Seitenanfang
6. Mögliche Probleme bei der Entsäuerung von Trinkwasser
Weiter Themenanfang Seitenanfang
5. Einsatzgrenzen von Calciumkarbonat
| Problembereiche | Arbeitsbereich |
| Eisengehalt | < |
| Temperaturbereich | 3 bis 35° |
| pH-Bereich | |
| Alkalinität | |
| Organische Stoffe | < 5 mg/lt |
| Öl | = 0 mg/ltr |
Nächstes Thema Zum Themenanfang Voriges Thema Zum Seitenanfang
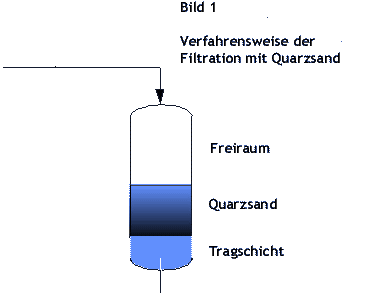
6. Verfahrensschema der Schnellfiltration mit Calciumkarbonat
Die Anwendung erfolgt in einem normalen
Filtrationsverfahren ( siehe Bild 1).
Durch ein periodisches Rückspülen wird das Filtrat ausgespült.
Nächstes Thema Zum Themenanfang Voriges Thema Zum Seitenanfang
7. Allgemeine Betriebsbedingungen der Schnellfiltration mit Calciumkarbonat
| Korngrößen in mm | 0,6 |
| Einsatzgebiet | Industrie |
| Schüttgewicht in kg/ltr | 1,4 |
| Filtergeschwindigkeit in m/h* | 7-12 abhängig von Anwendung |
| Rückspülung in m/h** | 45 |
| Rückspüldauer in Minuten | 20-30 |
| Stützschicht (Kies) in cm | 35 |
| Filterschichthöhe in cm | 75-90 |
| Freibord, % des Filterbetts | 35-50 |
* bei optimalen
Bedingungen, weiteres siehe Filtertechnik
** Die zusätzliche Anwendung von Luftspülung ist
vorteilhaft, wenn der Filterwiderstand um 0,2 bar zugenommen hat. Vor Einsatz
ist ein Test empfehlenswert.
Nächstes Thema Zum Themenanfang Voriges Thema Zum Seitenanfang
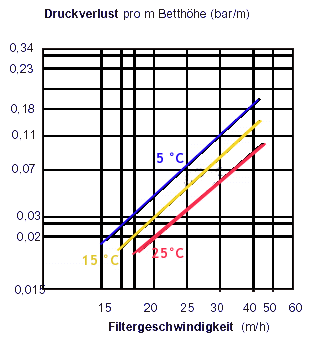
8. Druckverlust
Im untenstehenden Diagramm ist der Druckverlust in Abhängigkeit von der Filtergeschwindigkeit dargestellt. Ein Druckverlust von 0,5 bar sollte nicht überschritten werden. Spätestens bei Erreichen dieser Druckdifferenz ist eine Rückspülung durchzuführen
Nächstes Thema Zum Themenanfang Voriges Thema Zum Seitenanfang
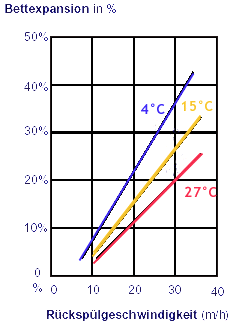
9. Bettausdehnung
Im untenstehenden Diagramm ist die Expansion des Filterbettes während der
Rückspülung dargestellt als Funktion der Wassertemperatur.
Die Rückspülung ist für 20 - 30 Minuten durchzuführen bei einer Bettexpansion
von 35 - 45%.
Nächstes Thema Zum Themenanfang Voriges Thema Zum Seitenanfang
7. Welcher Anlagentyp soll es sein
Weiter Themenanfang Seitenanfang
8. Was ist sonst noch beim Einsatz von Entsäuerungsanlagen zu beachten?
Seitenanfang Zu den Entsäuerungsanlagen
1. Marmorkies
Die notwendige Kiesmenge setzt sich aus Reaktions- und Verbrauchsmenge zusammen.
1. Reaktionsmenge
| Summe der gebundenen und freien Kohlensäure [mg/l] | 10 | 20 | 30 | 40 | 50 | 60 |
| Reaktionsmenge m³ je m³/h Durchlauf | 0,4 | 0,7 | 1,0 | 1,3 | 1,5 | 1,7 |
2.Verbrauchsmenge: 2,3 g Marmor/m³ Wasser/h für 1 mg/l = 1 g/m³ umgesetztem CO2 bzw. etwa 10mg/mmol umgesetztem CO2
Aufhärtung: 0,127°dH je mg/l umgesetztem CO2
Nachfüllzeit: 3 bis 6 Monate
Schüttgewicht: 1200 kg/m³ = 1,2 t/m³
Filterart: nur offene Filter üblich
Filterkiesschichthöhe: i.a. 1,0 bis 1,5 m (2,5 m)
Filtergeschwindigkeit: 0,6 bis 2,5 m/h
Reaktionszeit: 30 bis 270 min. für 10 bis 50 mg/l freier Kohlensäure
Dolomitisches Filtermaterial
Reaktionsmenge in Abhängigkeit vom Gehalt an aggressivem CO2 und Eisen für 1 m³/h Wasserdurchlauf
| Gehalt an freiem CO2 | bis 10 mg/l | 10 bis 20 mg/l | 30 mg/L |
|
Reaktionsmenge ohne Eisengehalt Reaktionsmenge mit Eisen bis 2 mg/l Reaktionsmenge mit Eisen über 2 mg/l |
180 kg 200 kg 225 kg |
225 kg 250 kg 275 kg |
250 kg 270 kg 300 kg |
Manganhaltiges Wasser erfordert zusätzlich 100 kg dolomitisches Filtermaterial für 1m³/h (alle Werte nur grobe Anhaltswerte).
Verbrauchsmenge
: 1,3 g/m³ Wasser/h für 1 mg/l umgesetztem CO2 bzw. etwa 55 mg/mmol CO2
Aufhärtung: 0,1 °dH je mg/l umgesetztem CO2 bzw. 0,7 mmol/l je mmol/l
umgesetztem CO2
Nachfüllzeit: 3 Monate bei kleinen Werken, sonst öfter bzw. es darf die festgelegte Schichthöhe durch den Verbrauch nicht um mehr als 10 % unterschritten werden
Schüttgewicht:1,1 bis 1,2 t/m³
Filterschichthöhen:
- offene Anlagen: 1,0 bis 2,0 mtr
- geschlossene Anlagen:1,5 bis 3,0 mtr (4,0 m)
Reaktionszeit: 10 bis 20 min. für 10 bis 90 mg/l freier Kohlensäure
Kalkhydrat
Verbrauchsmenge: 0,84 mg Ätzkalk, berechnet auf 100% Calciumoxydhydrat, je mg abgebundenem CO2
Aufhärtung: 0,064 ° d je mg/l abgebundenem CO2
Natronlauge
Verbrauchsmenge: 0,91 mg Ätznatron je mg CO2
Aufhärtung: keine Erhöhung der Karbonathärte

